Succinimid [123-56-8-A] C4H5NO2
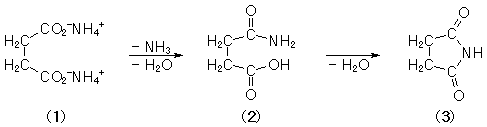
Zur Reaktion: Das zuerst gebildete Ammoniumsuccinat (1) zersetzt
sich beim Erhitzen in das Mono-Amid (2). Das entstandene Amid wird
durch die benachbarte Carboxylgruppe intramolekular zum cyclischen Imid (3), dem
Succinimid, acyliert.
Durchführung: Als Reaktionsapparatur dient ein 250-ml-Rundkolben mit
aufgesetztem Destillationsaufsatz samt Thermometer und absteigenden
Liebigkühler. Der Kühler wird ohne Kühlwasser als Luftkühler betrieben,
da das Succinimid bereits bei ungefähr 119 °C erstarrt. Im Kolben löst
man 39 g (0.33 mol) Bernsteinsäure durch langsame Zugabe von 50 ml
konzentriertem Ammoniak unter Schütteln und Kühlen. Anschließend werden
im Abzug durch Erhitzen etwa 40 ml Wasser abdestilliert. Beim weiteren
Erhitzen beginnt sich das feste Salz unter Ammoniakentwicklung zu
zersetzen, wobei die Temperatur am Thermometer nicht ansteigt. Erst
wenn die Temperatur der überdestillierenden Dämpfe bei stetigem
Weitererhitzen 105 °C erreicht hat, wechselt man die Vorlage und fängt
das bis 275 °C übergehende Destillat auf. Die bis 275 °C übergehende
Fraktion ist eine Mischfraktion. Das Succinimid destilliert ab 275 °C,
zum größten Teil zwischen 285-289 °C, und wird in einer neuen Vorlage
gesammelt. Es wird so lange weiter erhitzt, bis sich der restliche
Kolbeninhalt unter Dunkelfärbung zu zersetzen beginnt. Solbad sich aus
dem teerigen Rückstand gelbe Dämpfe entwickeln, wird die Destillation
gestoppt. Das erstarrte Destillat wird aus wenig eiskaltem Ethanol
umkristallisiert. Man erhält 25 g Succinimid als farblose Tafeln mit
einem Schmelzpunkt von 119-122 °C. Die Ausbeute beträgt 76% der
theoretisch erreichbaren Ausbeute. Das Präparat wird für die
Darstellung von N-Bromsuccinimid
benötigt.
Quelle: Gattermann, Ludwig - Die Praxis des Organischen Chemikers, 43.
Auflage, Walter de Gruyter, Berlin / New York 1982 • Organic
Syntheses, Coll. Vol. 2, p. 562
Delivered by: Mephisto
Letzte Aktualisierung: 20/04/06